近日,石藥集團產品線喜訊不斷:Claudin18.2 ADC完成海外授權,胃癌藥獲美國孤兒藥資格認定,2個神經領域藥品獲批……今年以來,石藥集團已有10個仿制藥、2個創(chuàng)新藥獲批上市。目前公司78個品種過評(21個首家),9個品種中選第七批集采;15個新注冊分類仿制藥在審,7個暫無首仿獲批;1類新藥瑞澤替尼、納樂舒單抗注冊申請在審,上市可期。
拿下10個重磅品種,78個過評品種亮眼
近日,石藥集團以仿制4類報產的加巴噴丁膠囊、拉考沙胺注射液獲批上市,并視同通過一致性評價。加巴噴丁膠囊、拉考沙胺注射液均為抗癲癇藥,石藥集團的拉考沙胺注射液為國產第二家。
2022年至今,石藥集團已經有10個新注冊分類仿制藥批產并視同過評,包括加巴噴丁膠囊、拉考沙胺注射液、氫溴酸伏硫西汀片、鹽酸普拉克索緩釋片、富馬酸丙酚替諾福韋片、多索茶堿注射液、鹽酸多奈哌齊片、注射用艾司奧美拉唑鈉、硝苯地平控釋片、甲磺酸侖伐替尼膠囊。其中,5個品種屬于神經系統(tǒng)藥物。
2022年至今石藥集團獲批上市的仿制藥
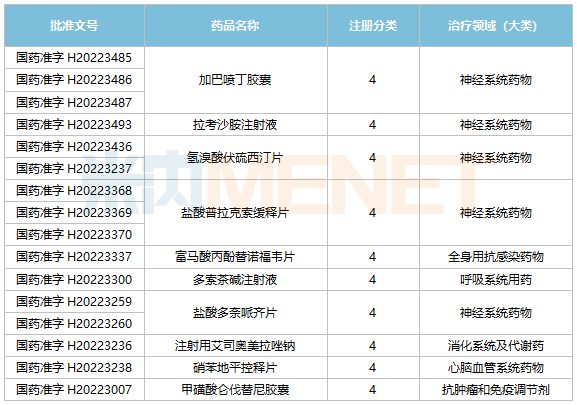
來源:米內網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫截至目前,石藥集團已經有78個品種通過/視同通過一致性評價。其中,21個品種為首家過評,鹽酸雷尼替丁膠囊、頭孢羥氨芐片、格列美脲分散片、雙嘧達莫片、乙磺酸尼達尼布軟膠囊、注射用兩性霉素B膽固醇硫酸酯復合物、鹽酸多柔比星脂質體注射液等7個品種為獨家過評。
石藥集團通過/視同通過一致性評價品種
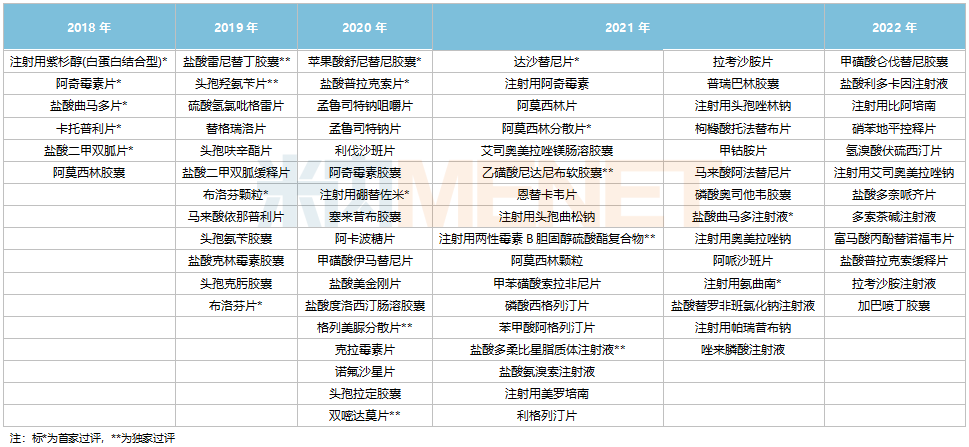
來源:米內網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫從治療領域來看,78個品種涵蓋8個治療大類,主要集中在全身用抗感染藥物(24個)、神經系統(tǒng)藥物(13個)、抗腫瘤和免疫調節(jié)劑(11個)和消化系統(tǒng)及代謝藥(11個)。
米內網(wǎng)數(shù)據(jù)顯示,2021年中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機構)終端抗腫瘤和免疫調節(jié)劑、消化系統(tǒng)及代謝藥市場規(guī)模均在1700億元以上,全身用抗感染藥物市場規(guī)模超過1500億元,神經系統(tǒng)藥物市場規(guī)模則超過1000億元。
9個品種中選第七批集采,6個過評品種蓄勢待發(fā)
7月18日,第七批集采中選結果正式公布,石藥集團有9個品種中選。其中,磷酸奧司他韋膠囊、甲磺酸侖伐替尼膠囊、拉考沙胺片、硝苯地平控釋片、唑來膦酸注射液等5個品種由于獲批時間短,石藥集團所占市場份額較低或空白,集采中選后有望迅速搶占市場。
石藥集團第七批集采中選情況
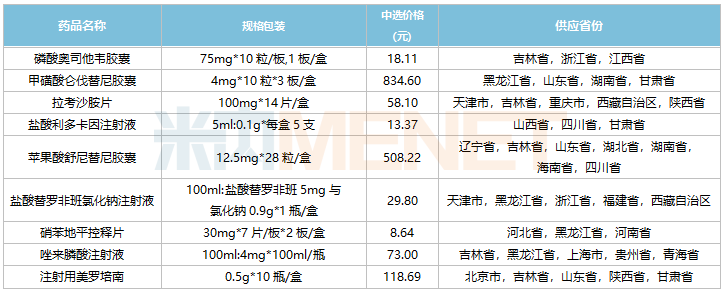
在國家開展的六批化藥集采中,石藥集團分別有1個、2個、9個、6個、3個、9個品種中標,合計30個品種。此前,石藥集團在2021年報中提及,多個新上市的仿制藥在國家集采中選及快速上量,帶來新的銷售收入貢獻,并使公司產品結構更為均衡。
除了被納入集采的品種,石藥集團還有16個過評品種暫未納入國家集采。
石藥集團已過評且暫未納入國家集采的品種

注射用比阿培南、氫溴酸伏硫西汀片、利格列汀片、注射用氨曲南、苯甲酸阿格列汀片、磷酸西格列汀片等6個品種過評企業(yè)+原研廠家達4家及以上,已經滿足了集采的“門檻”。其中,西格列汀、比阿培南、利格列汀等3個品種2021年在中國公立醫(yī)療機構終端銷售額分別超過18億元、8億元、6億元。
80余款創(chuàng)新藥、7個首仿沖刺,2款1類新藥上市可期
7月28日,石藥集團宣布,附屬公司石藥巨石生物已與Elevation就集團同類首創(chuàng)的抗Claudin 18.2抗體藥物偶聯(lián)物SYSA1801在大中華地區(qū)以外地區(qū)的開發(fā)及商業(yè)化訂立獨家授權協(xié)議。根據(jù)該協(xié)議的條款,石藥巨石生物將收取2700萬美元的首付款,并有權收取最多1.48億美元的潛在開發(fā)及監(jiān)管里程碑付款以及最多10.2億美元的潛在銷售里程碑付款。
這是石藥集團在Claudin18.2靶點上的第二次授權,2021年8月附屬公司NovaRock將創(chuàng)新藥物NBL-015(Claudin18.2單抗)海外獨家權利授予美國創(chuàng)新藥公司Flame,此次合作再次彰顯了石藥集團的研發(fā)實力。
目前,石藥集團研發(fā)管線豐富且完善,在腫瘤、免疫和呼吸、精神神經、代謝、心腦血管系統(tǒng)及抗感染等治療領域,擁有在研小分子創(chuàng)新藥40余項、大分子創(chuàng)新藥40余項、新型制劑30余項。
2022上半年,石藥集團創(chuàng)新藥產品線再添2個重磅新品,分別為鹽酸米托蒽醌脂質體注射液、度維利塞膠囊。其中,度維利塞膠囊是國內首款PI3K抑制劑,鹽酸米托蒽醌脂質體注射液是全球首個上市的米托蒽醌納米藥物。
2022H1石藥集團獲批上市的創(chuàng)新藥

值得一提的是,石藥集團還有甲磺酸瑞澤替尼膠囊、納樂舒單抗注射液2款1類新藥上市申請在審評審批中,上市可期。
石藥集團即將上市的1類新藥

2022年6月,石藥集團附屬公司津曼特的1類新藥RANKL單抗納樂舒單抗注射液提交上市申請并被納入優(yōu)先審評。該產品是全球首個報交的IgG4亞型全人源抗RANKL單克隆抗體,目前同靶點全球唯一上市藥物地舒單抗為IgG2亞型。米內網(wǎng)數(shù)據(jù)顯示,2021年地舒單抗全球銷售額為52.66億美元。甲磺酸瑞澤替尼膠囊是一款不可逆、高選擇性的第三代小分子EGFR-TKI,對EGFR敏感突變及EGFR T790M耐藥突變具有顯著的抑制活性。值得關注的是,瑞澤替尼上市申請已于2021年5月7日獲CDE承辦,有望于2022下半年獲批上市。
在仿制藥方面,石藥集團有15個新注冊分類品種報產在審,批產后將視同過評。其中,7個品種暫無首仿(含劑型首仿)獲批上市,包括伊立替康脂質體注射液、培唑帕尼片、琥珀酸去甲文拉法辛緩釋片、阿普米司特片、瑪巴洛沙韋片、坎地沙坦酯氨氯地平片、沙庫巴曲纈沙坦鈉片。
石藥集團在審的新注冊分類仿制藥
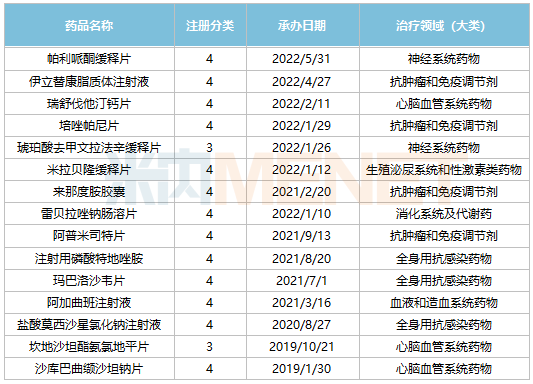
來源:米內網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
伊立替康脂質體注射液、瑪巴洛沙韋片、坎地沙坦酯氨氯地平片等3個品種由石藥集團獨家以新注冊分類仿制藥報產。其中,伊立替康2021年在中國公立醫(yī)療機構終端銷售額接近19億元,作為該品種新制劑,伊立替康脂質體注射液將對該品種市場帶來沖擊。
數(shù)據(jù)來源:米內網(wǎng)數(shù)據(jù)庫、公司公告注:米內網(wǎng)《中國公立醫(yī)療機構終端競爭格局》,統(tǒng)計范圍是:中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院,不含民營醫(yī)院、私人診所、村衛(wèi)生室;上述銷售額以產品在終端的平均零售價計算。數(shù)據(jù)統(tǒng)計截至8月1日,如有疏漏,歡迎指正!

