日前,恒瑞醫(yī)藥以仿制4類報產(chǎn)的吸入用七氟烷進入行政審批階段。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年中國公立醫(yī)療機構(gòu)終端吸入用七氟烷銷售額超過20億元,同比增長8.71%。目前該產(chǎn)品還未有企業(yè)過評。
圖1:恒瑞吸入用七氟烷注冊進度
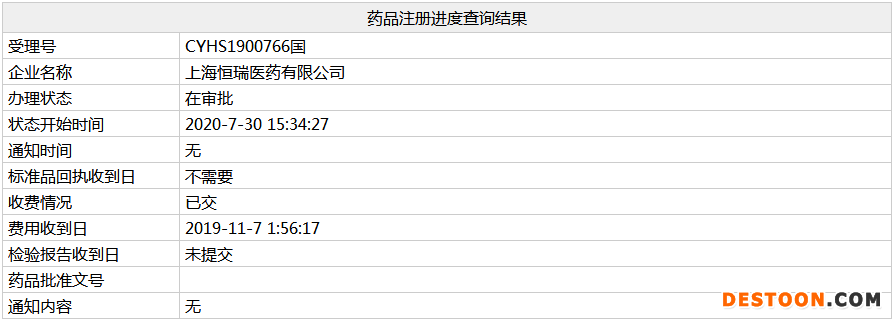
吸入用七氟烷是一種鹵代吸入性全身麻醉劑,臨床上適用于成人和兒科患者院內(nèi)手術(shù)及門診手術(shù)的全身麻醉的誘導和維持。該產(chǎn)品最早由雅培公司研發(fā),于1995年6月在美國獲批上市,專利已過期很多年,百特和印度Piramal公司的七氟烷仿制藥分別在2002年7月和2007年5月在美國獲批上市。
目前國內(nèi)有6家企業(yè)(3家國產(chǎn),3家進口)擁有吸入用七氟烷生產(chǎn)批文,米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機構(gòu))終端吸入用七氟烷銷售額超過20億元,同比增長8.71%。
表:吸入用七氟烷一致性評價申報情況
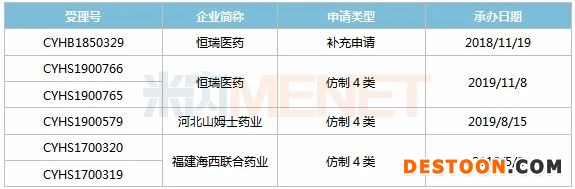
3家企業(yè)布局吸入用七氟烷一致性評價,恒瑞醫(yī)藥既提交了一致性評價補充申請,又以新分類報產(chǎn),受理號CYHS1900766已進入新政審批階段;河北山姆士藥業(yè)、福建海西聯(lián)合藥業(yè)以新分類提交吸入用七氟烷上市申請。
2015年11月10日,恒瑞醫(yī)藥發(fā)布公告稱,公司生產(chǎn)的吸入用七氟烷通過美國FDA認證,獲準在美國市場銷售。通過“國外轉(zhuǎn)報國內(nèi)”的方式,恒瑞以國外注冊申請的相關(guān)資料在國內(nèi)進行申報,無需再進行BE試驗。受益于該方式,公司的另一款吸入劑吸入用地氟烷已于2018年7月獲批生產(chǎn),雖然是按仿制藥6類申報,但已納入《中國上市藥品目錄集》,因此視同通過一致性評價。
圖2:吸入劑過評情況
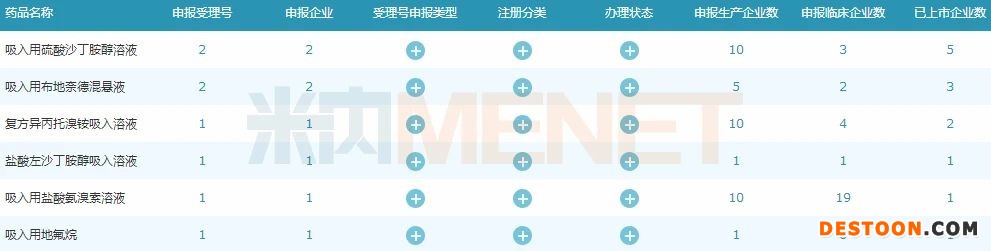
米內(nèi)網(wǎng)數(shù)據(jù)顯示,目前6個吸入劑已有企業(yè)過評,其中吸入用硫酸沙丁胺醇溶液、吸入用布地奈德混懸液過評企業(yè)數(shù)均達2家;除了韓美藥品的吸入用鹽酸氨溴索溶液,其余5個均為國產(chǎn)吸入劑。
6個過評吸入劑中有5個為呼吸系統(tǒng)用藥,吸入用硫酸沙丁胺醇溶液、吸入用布地奈德混懸液、復方異丙托溴銨吸入溶液、鹽酸左旋沙丁胺醇吸入溶液均為抗哮喘藥,吸入用鹽酸氨溴索溶液為咳嗽與感冒用藥;恒瑞醫(yī)藥的吸入用地氟烷為神經(jīng)系統(tǒng)藥物,用于麻醉誘導和麻醉維持。
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫、國家藥監(jiān)局
注:數(shù)據(jù)統(tǒng)計截至8月6日,如有疏漏,歡迎指正!



 110102000668(1)號
110102000668(1)號