1月21日訊 1月20日,東陽光藥兩款創(chuàng)新藥的臨床申請獲得CDE承辦受理,分別為1類新藥HEC88473注射液及3.3類新藥德谷胰島素注射液。在剛剛過去的2020年,東陽光藥有1個3.3類新藥申請上市,9個新藥申請臨床(7個為1類新藥),其中6個已獲批臨床。
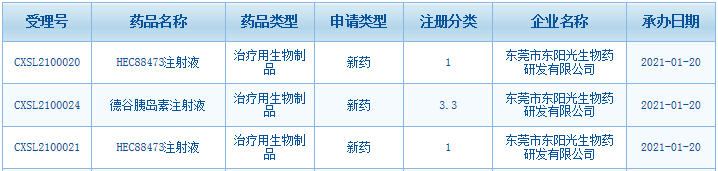
來源:CDE官網(wǎng)
HEC88473注射液是東陽光藥2021年首個提交臨床申請的1類新藥;德谷胰島素注射液是一種新型的、超長效應(yīng)的胰島素類似物,2019年全球銷售額超過15億美元;2020年上半年在中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機構(gòu))終端銷售額超過5000萬,同比增長922.6%。
在過去的2020年,東陽光藥有1款新藥申請上市,為甘精胰島素注射液,米內(nèi)網(wǎng)數(shù)據(jù)顯示,2020年上半年中國公立醫(yī)療機構(gòu)終端甘精胰島素銷售額超過30億元。
此外,7款1類新藥、2款2類改良型新藥申請臨床,其中HEC95468片、重組抗VEGF人源化單克隆抗體注射液、HEC122505MsOH片、HEC89736PTSA·0.5H2O片、對甲苯磺酸寧格替尼膠囊、鹽酸伊非尼酮片已獲批臨床。
2020年東陽光藥創(chuàng)新藥申報情況
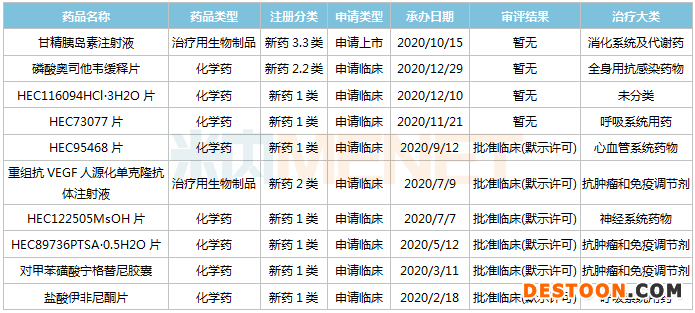
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
1類新藥中,HEC89736PTSA·0.5H2O片是東陽光藥自主研發(fā)的口服高選擇性PI3Kδ抑制劑,擬用于治療血液腫瘤;HEC122505MsOH片為神經(jīng)系統(tǒng)藥物,目前已啟動I期臨床;對甲苯磺酸寧格替尼膠囊和鹽酸伊非尼酮片非首次獲批臨床。
2類新藥中,重組抗VEGF人源化單克隆抗體注射液為貝伐珠單抗生物類似藥,目前國內(nèi)已有信達、齊魯兩家企業(yè)的生物類似藥獲批上市。
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫、CDE官網(wǎng)
注:數(shù)據(jù)統(tǒng)計截至1月20日,如有疏漏,歡迎指正!



